妊娠、输血、多次器官移植病史均可以导致尿毒症患者体内产生群体反应性抗体(PRA),高PRA的尿毒症患者在寻找配型合适的供体时往往面临很大困难,常因存在预存供者特异性抗人白细胞抗原(HLA)抗体而失去移植机会。此外,预存供者特异性抗体(DSA)阳性患者在术后早期更容易发生急性抗体介导的排斥反应,移植失败的风险也相对较高。郑州大学第一附属医院肾移植科回顾性分析15例DSA阳性患者肾移植术前及术后处理方案,探讨DSA阳性肾移植的可行性与脱敏方案的作用与安全性,结果表明,经过有效的术前预处理进行脱敏治疗能够有效预防DSA阳性肾移植抗体反弹,减少围手术期并发症的发生。现摘录相关内容以供学习参考。
一、研究对象
回顾性分析2017年8月~2022年7月开展的15例术前预存DSA阳性肾移植受者的临床资料。
纳入标准:(1)在我科接受亲体器官捐献或已故供体肾移植的成人患者(18岁及以上);(2)临床资料完整,实验室相关化验完整;(3)在术前和术后定期检测HLA抗体;(4)有供者的HLA分型;(5)随访时间3个月以上。
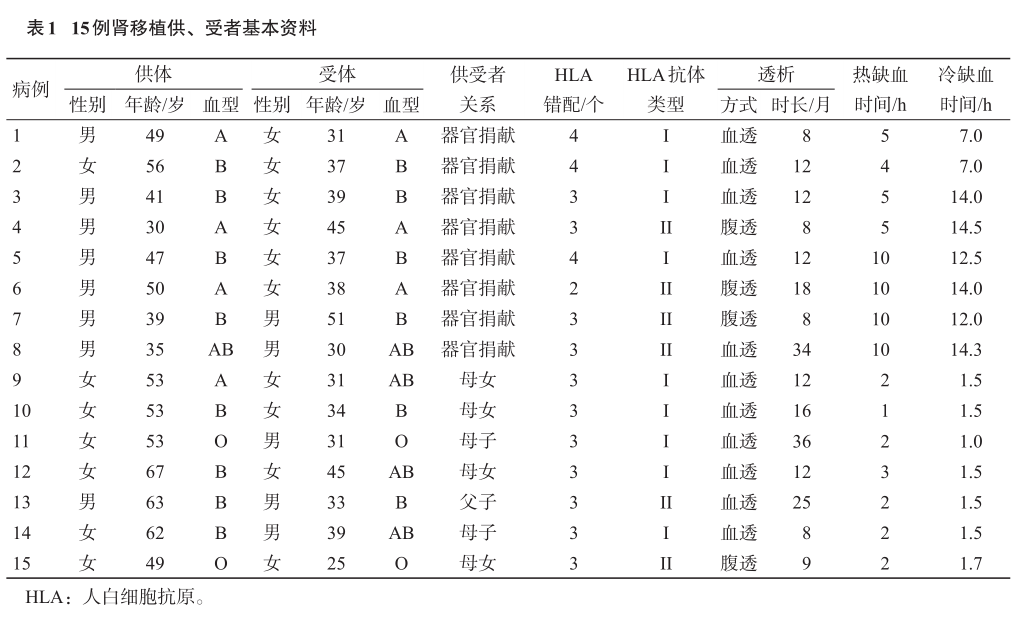
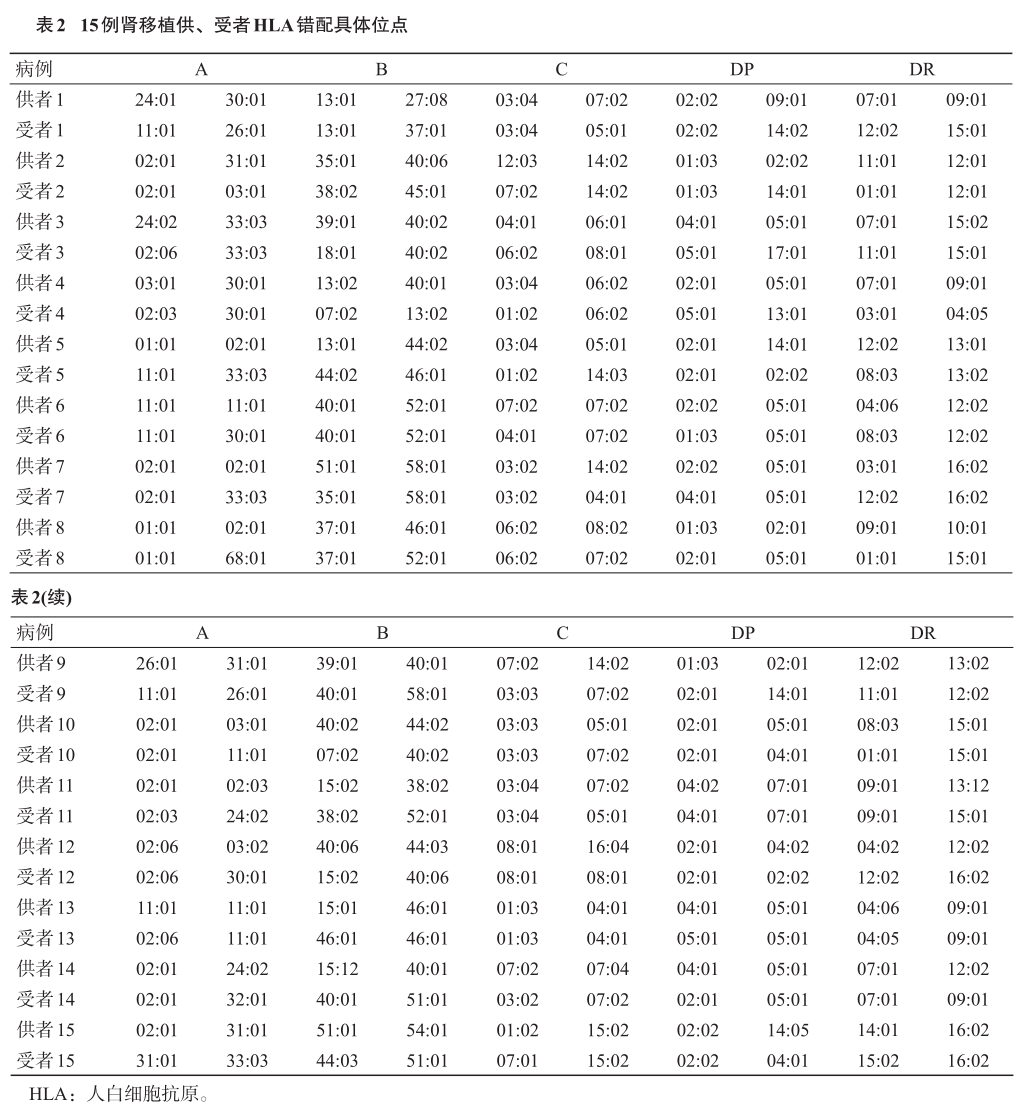
15例供、受者基本资料见表1。15例受者中男性5例,女性10例;移植时年龄25~51岁,平均年龄36.4岁;器官捐献来源肾移植8例,亲属活体肾移植7例;1例受者为二次肾移植,其余均为首次肾移植;受者原发病中不明原因14例,IgA肾病1例;术前血液透析11例,腹膜透析4例,透析时间为8~36个月;预存HLAI类抗体9例,预存HLAII类抗体6例,HLA错配的具体位点见表2。
DSA平均荧光强度(MFI)的判定分层标准:(1)阴性,MFI<500;(2)弱阳性,MFI为500~3999;3)中阳性,MFI为4000~10000;4)强阳性,MFI>10000。
二、器官来源及受者预处理方案
(一)器官捐献肾移植受者预处理
8例为公民逝世后器官捐献(DCD)来源受者(病例1~8),术前PRA、DSA均阳性,淋巴毒交叉实验均阴性。
DCD未处理组3例:病例1~3未进行脱敏处理,于手术当天给予甲泼尼龙+即复宁进行免疫诱导治疗;
DCD预处理组5例:病例4~8根据患者体重水平于术中开放吻合血管前给予利妥昔单抗(<50kg的患者为100mg,≥50kg的为200mg)清除B细胞进行脱敏治疗,同时使用甲泼尼龙及即复宁行免疫诱导治疗。
(二)亲属活体肾移植受者预处理
LRD预处理组7例:7例为亲属活体供者(LRD)肾移植受者(病例9~15),术前PRA、DSA均为阳性,淋巴毒交叉实验均为阴性。术前50d根据患者体重给予患者利妥昔单抗(<50kg的患者为100mg,50~65kg的为200mg,>65kg的为300mg),并通过淋巴细胞免疫分析技术了解B细胞变化水平;术前1~2周根据患者DSA的MFI水平给予患者3~6次血浆置换降低患者体内预存DSA水平,并提前1~2周开始口服免疫抑制剂他克莫司(TAC)+吗替麦考酚酯(MMF)。手术当天暂停服用TAC+MMF,接受甲泼尼龙(<50kg的患者为750mg,≥50kg为1000mg)联合兔抗人胸腺免疫球蛋白的免疫诱导治疗。
(三)受者免疫维持方案
所有受者术后第1~6天甲泼尼龙逐渐减量,分别为500、375、250、160、80、40mg,术后第7天改为每天口服甲泼尼龙片12mg,逐渐减少剂量后维持于每天4~8mg。术后1~4d即复宁的初始剂量为每天25~50mg并根据受者的免疫状态调整剂量。其中围手术期甲泼尼龙总用量为1500~2000mg,即复宁总用量为150~250mg。术后第2天开始恢复TAC+MMF的使用(TAC的浓度维持在8~10ng/mL)。
三、结果
(一)DCD受者术后肾功能及DSA水平
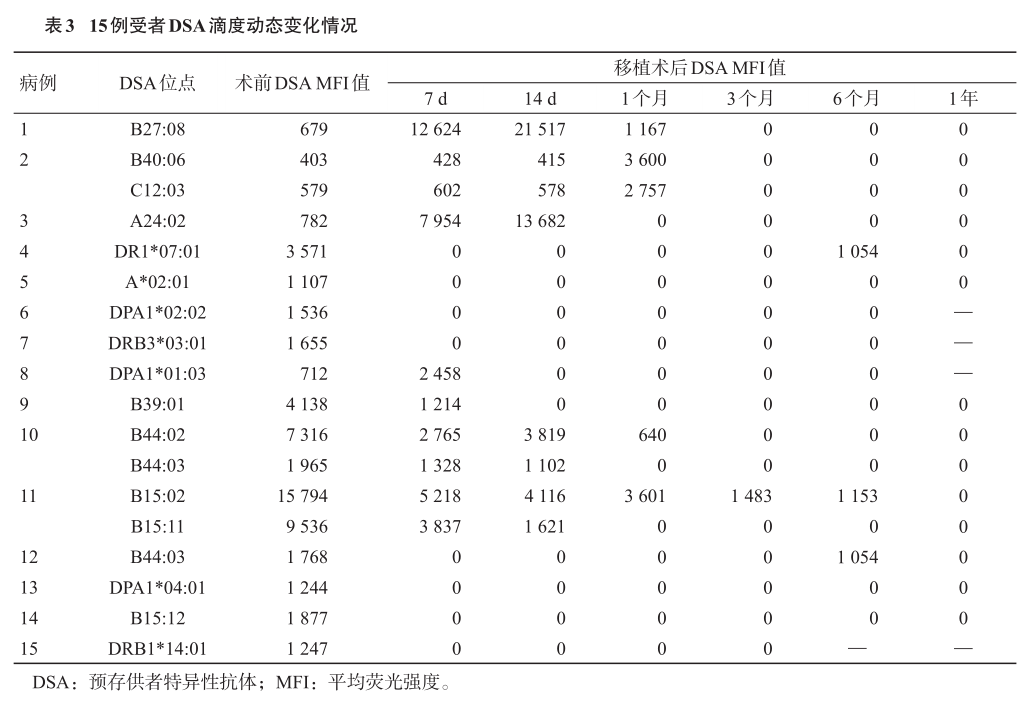
DCD未处理组:3例受者术后均出现DGF,复查PRA发现3例受者DSA MFI值均发生反弹(表3),初步怀疑由抗体介导的排斥反应所致移植肾功能延迟恢复(DGF)。1例(病例3)给予甲泼尼龙+即复宁冲击并联合静脉注射利妥昔单抗200mg等治疗后好转,其余2例(病例1、2)受者给予多次血浆置换,联合应用静脉注射免疫球蛋白(IVIG)(每天10g)加利妥昔单抗200mg治疗后DSA水平下降,血肌酐和尿量逐渐恢复正常。
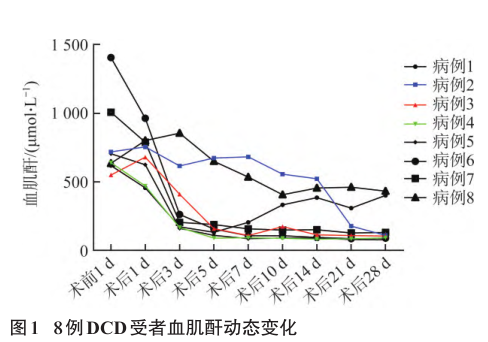
DCD预处理组:5例受者中,4例受者的血肌酐值稳定下降(图1),并未出现排斥反应、凝血功能异常、感染等相关并发症,并于术后2周左右顺利出院。
病例8术后1d出现尿量减少,血肌酐处于高值水平,最高达到855μmol/L,复查PRA示DSA MFI值较术前升高(DPA1*01:03,MFI值712→5768),初步考虑为抗体介导的排斥反应导致的DGF。遂于术后1~10d行4次血浆置换,治疗后血肌酐仍处于高值水平,在术后第16、20、22天行3次血液透析后于术后25d在局麻下行移植肾病理活检,移植肾穿刺病理结果显示移植肾急性肾小管损伤,不排除急性活动性抗体介导的排斥反应,穿刺后继续行血液透析2次,患者尿量和肾功能逐渐恢复,术后45d血肌酐降至97μmol/L并出院。
(二)LRD受者术后肾功能及DSA水平
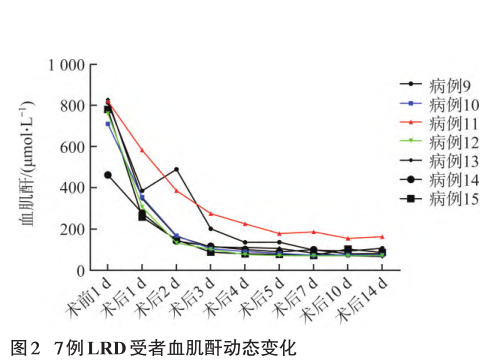
LRD预处理组:7例受者经过处理使PRA、DSA水平明显下降后进行移植,其中6例受者的血肌酐值逐步降低(图2),且均未出现排斥反应、凝血功能异常、感染等相关并发症,并于术后2周左右顺利出院。
1例受者于术后13d发现尿量减少及血肌酐升高,复查PRA发现DSA MFI值回升,给予甲泼尼龙250mg冲击治疗2d后尿量恢复,复查肾功能示血肌酐水平恢复到正常水平。
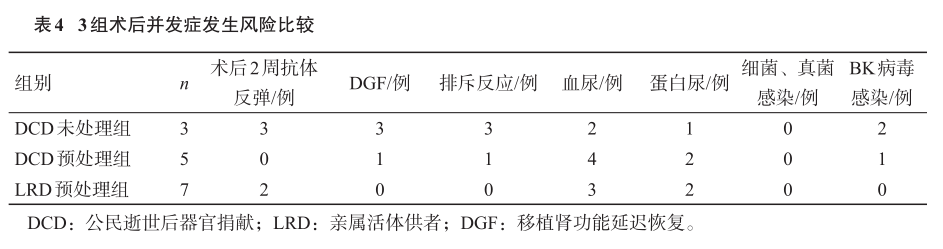
(三)术后并发症
对比DSA抗体反弹情况,术后2周DCD未处理组3例患者均发生抗体反弹,DCD预处理组均未发生抗体反弹。DCD未处理组患者DGF、排斥反应的发生率均高于DCD预处理组和LRD预处理组。3组术后患者血尿、蛋白尿、细菌真菌感染率及BK病毒感染率的差异均无统计学意义(均P>0.05,表4),表明经过有效的抗感染预防和治疗后预后良好。
(四)受者及移植肾存活情况
15例受者随访至2022年10月,随访时间为3~60个月,中位值为21个月。其中随访1年以上11例,3年以上6例,5年以上1例,受者和移植肾存活率均为100%(15/15)。
四、讨论
尿毒症患者在移植前接触其他外源性抗原时体内会产生抗HLA抗体,当这些预先存在的抗HLA抗体遇到移植物表达的相同抗原时,机体便会启动针对移植物的超急性或急性排斥反应。因此,预存DSA阳性尿毒症患者过往被认为是肾移植的相对禁忌证之一,而针对这类尿毒症患者的脱敏治疗一直是移植领域关注的热点。
脱敏治疗是通过物理或药物的方式清除患者循环中的DSA,并靶向作用于T、B细胞,阻止DSA合成,从而防止超急性或急性排斥反应的发生,使这些预存DSA阳性尿毒症患者能够成功接受肾移植。目前用于临床脱敏治疗策略主要包括以下几种方式:抗CD20单抗(利妥昔单抗)清除B细胞、血浆置换清除外周血循环中的DSA、使用IVIG进行免疫调节,同时联用有效的诱导治疗及维持免疫抑制方案。
利妥昔单抗是一种靶向作用于B细胞表面分子CD20的单克隆抗体,可以快速清除表达CD20的B细胞,从而抑制抗体及细胞因子生成以及抗原提呈细胞激活。B细胞在骨髓中发育,经历功能性B细胞受体的表达和自身免疫耐受的形成,最后分化为表达CD20的初始B细胞进入血液和外周淋巴器官。初始B细胞在外周循环中经历2种命运,若无抗原刺激,初始B细胞的寿命只有7~10d;若受到抗原刺激后,初始B细胞经过一系列突变、筛选和扩增后产生浆细胞或进入生发中心形成记忆B细胞,这类浆细胞寿命很短,一般只能存活数天,而记忆B细胞寿命很长,甚至可以伴随终生。利妥昔单抗因其对CD20阳性B细胞的杀伤作用在肾移植中被广泛应用于高致敏患者的脱敏、急性和慢性抗体介导的排斥反应以及肾移植术后复发和新发肾小球疾病等的治疗。利妥昔单抗建议在移植前2周或更早使用,这种提前清除外周初始B细胞和记忆B细胞的治疗可以避免受者在接触移植物时体内存在的大量B细胞分化为浆细胞并产生大量抗体。利妥昔单抗的应用剂量尚无统一标准,本研究通过前期开展ABO血型不相符肾移植发现,根据患者体重应用利妥昔单抗即可有效清除受者外周血B细胞,不再需要增加利妥昔单抗的临床剂量,从而降低术后感染发生率及治疗费用。由于器官捐献来源和供肾时间无法把握,本研究中早期的3例受者均未使用利妥昔单抗进行脱敏治疗,均出现抗体介导的排斥反应导致DGF,后期发现术前提前应用适当剂量的利妥昔单抗可以在一定程度提高手术的成功率并且降低排斥反应的发生率。但是利妥昔单抗并不能有效去除生发中心记忆B细胞和骨髓中的长寿命浆细胞,生发中心记忆B细胞和长寿命浆细胞也可以分泌DSA,因此在使用利妥昔单抗的同时也要定期检测患者的DSA水平。
血浆置换是通过物理方法非选择性地将大分子物质,例如抗体、补体、免疫复合物和凝血因子等从血浆中去除。血浆置换是清除DSA最快的方式,抑制抗体产生的疗法往往需要数周或数月才能生效,而血浆置换则可以短时间内快速去除DSA,特别是对于HLAI类抗体清除效果更好。但血浆置换并未作用于产生抗体的B细胞,所以在治疗后数周内抗HLA抗体往往会发生反弹,甚至恢复至基线水平,因此需要联用其他方法进行脱敏治疗。但是在和利妥昔单抗联用时,血浆置换可以降低利妥昔单抗的血浆浓度,所以血浆置换最好在1~2个利妥昔单抗半衰期后使用,即利妥昔单抗于术前50d左右应用,而血浆置换于术前2周应用,充分保证2种治疗方案均达到最佳的治疗效果,本研究中的亲属活体肾移植患者即采用此种方案。
IVIG是从血浆中提取的IgG的混合物,可以中和抗体,抑制炎症细胞因子的产生,抑制补体成分的结合,也可以改变抗原提呈细胞和B细胞的活性,抑制B细胞发育和成熟。在使用IVIG时,本研究采用术后第1周每天20g,术后第2周每天10g,降低DSA滴度的同时可以有效预防术后感染发生。
联合使用利妥昔单抗+血浆置换+IVIG+免疫抑制剂的治疗方案可以在一定程度上降低抗体介导的排斥反应(AMR)的发生风险,提高预存DSA尿毒症患者的移植肾存活率以及改善预后。本研究病例1~3为DCD受者,术前PRA、预存DSA阳性,早期并未进行相关脱敏预处理,仅给予常规诱导冲击治疗后行肾移植术,术后均发生AMR导致DGF。经过血浆置换联合利妥昔单抗、IVIG、甲泼尼龙等脱敏治疗后,3例受者尿量及肾功能亦逐渐恢复至正常水平,提示对预存DSA阳性需进行预处理后再进行肾移植手术更为安全。对预存DSA阳性的DCD来源受者根据患者体重应用利妥昔单抗,除病例8出现AMR导致的DGF外,其余4例均未出现排斥反应等并发症,术后肾功能恢复良好并均于术后2周左右出院。病例9~15均为LRD受者,术前PRA、预存DSA阳性,围手术期经过充分的预处理,即利妥昔单抗+血浆置换+大剂量IVIG+提前应用口服免疫抑制剂等联合治疗方案,有效降低受者体内PRA以及预存DSA水平,除病例10出现激素敏感的亚临床排斥反应外,其余6例均未出现排斥反应,术后移植肾功能恢复良好。
DSA是由于HLA不匹配而产生的,HLA按其分布和功能分为I类抗原、II类抗原和III类抗原。在肾移植配型中,主要针对的是经典的HLAI类和II类抗原。本研究15例患者中,9例为HLA I类DSA,6例为HLA II类DSA。6例HLA II类DSA均为抗HLA-DP或HLA-DR抗体,术前DSA总体MFI值为1766,由于II类抗体阳性患者对各种治疗方案相对不敏感,因此本研究选择的都是II类抗体滴度相对较低的患者。DSA引起的AMR有2种形式,1型AMR是由致敏患者中先前存在的供者特异性抗体的持续存在或反弹引起的,通常发生在移植后早期,1型AMR与抗I类HLA、II类HLA抗体相关;2型AMR与新生DSA相关,通常发生在移植后1年以上,与1型AMR相比,2型AMR发生较晚,与II类HLA的DSA更为相关,特别是出现抗HLA-DQ抗体时,且新生DSA导致的慢性AMR往往治疗效果相对较差,往往是移植肾功能丢失的主要原因。而预存DSA会使早期AMR治疗效果好,长期随访的结果也好,特别是当预存DSA为抗HLA I类抗体,患者对血浆置换等治疗方式更为敏感,预后也相对较好。
由于围手术期应用利妥昔单抗+血浆置换+即复宁这些免疫抑制药物后,肾移植受者的淋巴细胞绝对值降低,患者发生感染的概率大大增加;术后随访期间MMF用量相对要减量。此外,利妥昔单抗应用后半年内患者B细胞绝对数量均在较低水平,患者发生耶氏肺孢子菌感染的概率大大增加,由于复方磺胺甲噁唑同时具有抑菌和杀菌作用,并且毒性小、价格便宜,本研究在随访过程中根据患者淋巴细胞绝对值长时间使用复方磺胺甲噁唑预防感染,应用时间普遍在1年以上,随访期间未见感染发生率升高。
本研究的初步经验表明,术前预存DSA阳性的患者经过术前和术后脱敏治疗后可以成功地进行肾移植手术。同时要加强术后对DSA的常规检测,防止抗体效价的反弹以及及早进行处理。但是本研究样本量相对较少,仍需不断总结临床经验,继续深入研究。
本文仅供学习参考,完整准确内容请查阅原始文献:樊红召,刘佳,孙佳佳,王军祥,庞新路,尚文俊,丰贵文,李金锋.15例预存供者特异性抗体阳性肾移植的临床特征[J].中南大学学报(医学版),2023,48(10):1583-1591.
【链接】
肾移植术后抗体检查:群体反应性抗体和供者特异性抗体
http://yizhiwang.org.cn/forum.php?mod=viewthread&tid=87335
《肾脏移植术前准备操作指南(2023版)》17条推荐意见概览
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=89711
《中国肾脏移植组织配型临床诊疗指南(2023版)》21条推荐意见概览
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=89663
肾移植等待者抗HLA抗体阳性的CALM应对策略
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=87398
《肾脏移植免疫监测临床诊疗指南(2023版)》24条推荐意见概览
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=89635
|